原创 化学柯老师 化学柯老师 2025年01月20日 07:05 北京
一、问题的由来
前段时间,网络上有人讨论过“等浓度的CH3COONa和NaHCO3溶液的pH大小比较”的问题。我想问各位,如果您的学生问您这个问题,您如何回答?我估摸着不少人会这么思考和回答:由于CH3COONa和NaHCO3都是强碱弱酸盐,在水溶液中都会发生水解反应,生成对应的酸和氢氧根离子,从而使溶液呈现碱性。都说“越弱越水解”,由于酸性:CH3COOH>H2CO3,从而CH3COO−的水解程度小于HCO3−的水解程度,所以相同温度下,CH3COONa溶液和等浓度的NaHCO3的溶液相比,前者水解产生的OH−浓度小于后者,所以碳酸氢钠溶液的pH大。是不是真的这样呢?
二、实验测定结果和理论计算分析
也有人专门通过计算,室温下,0.1mol∙L−1CH3COONa溶液的pH=8.88,而0.1mol∙L−1NaHCO3溶液的pH=8.31。这个结果,和根据“越弱越水解”的水解规律正好相反,出乎意料吧?前者相对好算,我也算出来了;后者真不好算,我算了半天,还真没算出来。我们知道,室温下饱和NaHCO3溶液的pH约为8.4,“室温下,0.1mol∙L−1NaHCO3溶液的pH=8.31”这个结果应该不会差。看来“越弱越水解”在碰到像NaHCO3这样的多元弱酸酸式盐时失灵了呀,还真是要慎用呀。那是不是就能认为相同条件下,碳酸氢钠溶液的pH一定比等浓度的CH3COONa溶液小呢?
我想起朱建民老师发表在《科教导刊·电子版》2018年第22期的文章《碳酸氢钠溶液的pH与其浓度关系探讨》。

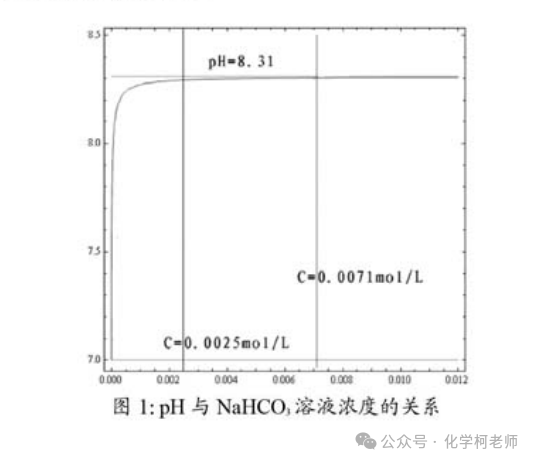
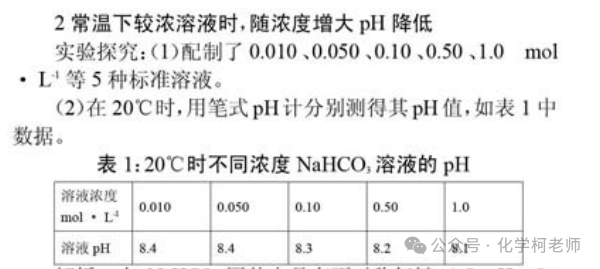
根据朱老师的计算和实验结果,室温下NaHCO3稀溶液的pH区间为7<pH≤8.31,其中当NaHCO3溶液浓度大于0.0025mol∙L−1时,其pH基本保持不变,约为8.31。而NaHCO3溶液浓度较大时,随浓度增大pH降低。而室温下随浓度增大,CH3COONa溶液pH增大,那么当CH3COONa溶液的pH=8.31时,对应的浓度是多少呢? 我经过计算得此时CH3COONa溶液的浓度约为0.0071mol∙L−1,在朱老师的pH与NaHCO3溶液浓度关系图上,叠加一条pH与CH3COONa溶液浓度关系的曲线,这条曲线经过(0.0071,8.31)、(0.1,8.88)两个点。这两条曲线是图上浓度对应范围内是有交点的,也就是说:当浓度大于0.0071mol∙L−1时,CH3COONa溶液的pH大;当浓度等于0.0071mol∙L−1时,两者溶液的pH一样大,都约为8.31;当浓度小于0.0071mol∙L−1时,会出现NaHCO3溶液的pH要大一些的情况(当然极稀情况下,两者大小关系还有可能出现反复)。因此抛开浓度大小,还真没法去比较“等浓度的CH3COONa和NaHCO3溶液的pH大小”。
这里笔者想到了多年前的一道高考题:

这么看来,十年前这道高考题的D项在命题时就不严谨了。
唉,NaHCO3真是让人又爱又恨呀!
那到底为什么NaHCO3溶液会这么反常呢?
三、微观解释——自偶电离的提出
一般地,除了水的电离平衡,在分析NaHCO3溶液时,我们一般会考虑HCO3−的水解、电离两个平衡,即
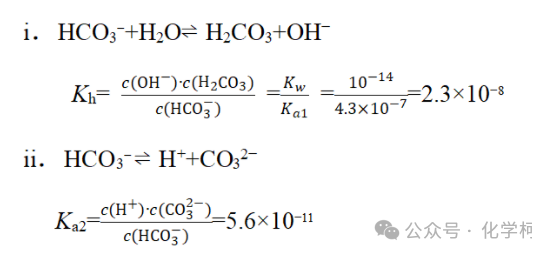
由于Kh>Ka2,溶液中c(OH−)>c(H+),所以NaHCO3溶液呈碱性。但是仅考虑HCO3−的水解、电离,在比较NaHCO3溶液其他粒子浓度大小时就会出现问题,多年前就出现过两种观点:
①c(Na+)>c(HCO3−)>c(OH−)>c(H+)>c(CO32−);
②c(Na+)>c(HCO3−)>c(OH−)>c(CO32−)>c(H+)。
这两种观点的分歧在于c(CO32−)和c(H+)的大小,争论很久,谁也说服不了谁。那好吧,就搁置争议吧,于是试题和教学中都刻意回避了这一点。其实,持有这两种观点的人都忽略了溶液中HCO3−与HCO3−之间的相互作用。通过上面讨论,由i 式和ii式可知,HCO3−会电离出H+,而同时,HCO3−也会结合水电离出来的H+;HCO3−在溶液中运动时是会碰到其他的HCO3−,既然质子的受体和给体能发生碰撞,那么HCO3−也会结合溶液中另一部分HCO3−电离出的H+,即发生反应iii.HCO3−+HCO3−⇌H2CO3+CO32− (类似于水的自偶电离,我们姑且称反应iii为HCO3−的自偶电离吧),HCO3−的自偶电离反应进行程度有多大呢?我们来计算一下反应iii的平衡常数
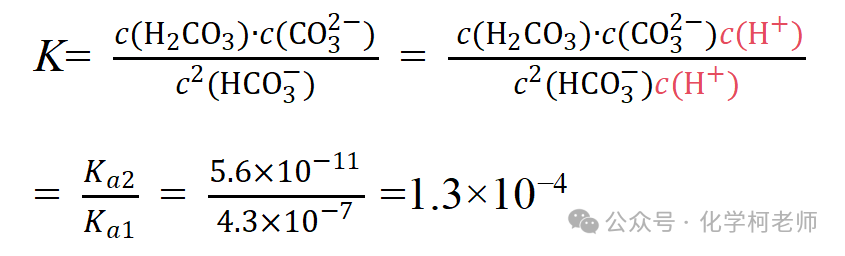
对比反应i、ii、iii的平衡常数不难发现,反应iii进行的程度远远大于反应i和ii,而反应i进行的程度又大于反应ii,因此NaHCO3溶液中的离子浓度大小关系应为c(Na+)>c(HCO3−)>c(CO32−)>c(OH−)>c(H+)。当然,如果是极稀的溶液中,无法忽略水的电离的影响时,这个排序又需要重新考虑了。
再回到最开始“等浓度的CH3COONa和NaHCO3溶液的pH大小比较”那个问题,为什么不同浓度下会出现三种不同的结果呢?
笔者斗胆从微观上作一下解释的尝试:CH3COONa溶液体系相对简单,pH的变化主要体现在浓度的改变对水解平衡的影响,而NaHCO3溶液体系则要复杂的多,存在着多个平衡,且每个平衡之间既相互联系、又相互制约。当NaHCO3溶液浓度较大时,随NaHCO3溶液浓度的增加,HCO3−和HCO3−发生碰撞的几率增大,即发生反应iii为主,抑制了反应i和ii,再加上HCO3−间氢键的缔合作用程度逐渐增大,导致发生电离与水解的HCO3−量进一步减少,使得碱性反而不如等浓度的CH3COONa溶液大。当NaHCO3溶液较稀时,HCO3−和HCO3−发生碰撞的几率减小,同时HCO3−和水分子发生碰撞的几率增大,即反应iii对反应i和ii的抑制作用越来越小,此时“越弱越水解”才算有了用武之地。在NaHCO3溶液浓度变化的过程中会出现一个临界点:就是当浓度等于0.0071mol∙L−1时,两者溶液的pH一样大,都约为8.31。
当然我这个解释还需要更多的数据支撑,有一些计算还需要更精准些。一家之言,不一定对,欢迎更多的人参与讨论。
后记:
其实早在去年讨论2023年福建卷第10题时我就思考过这个问题,由于思考不成熟,迟迟没有动笔,前两天见到网传的2025年浙江一月化学首考15题,高考题再次把手伸向NaHCO3了,这次是有备而来。嗯,是时候出手了!

评论详情