1. 沸点和熔点
氢键能显著提高物质的沸点和熔点。例如,水(H₂O)的沸点远高于硫化氢(H₂S),因为水分子间存在较强的氢键,而硫化氢分子间主要是较弱的范德华力。
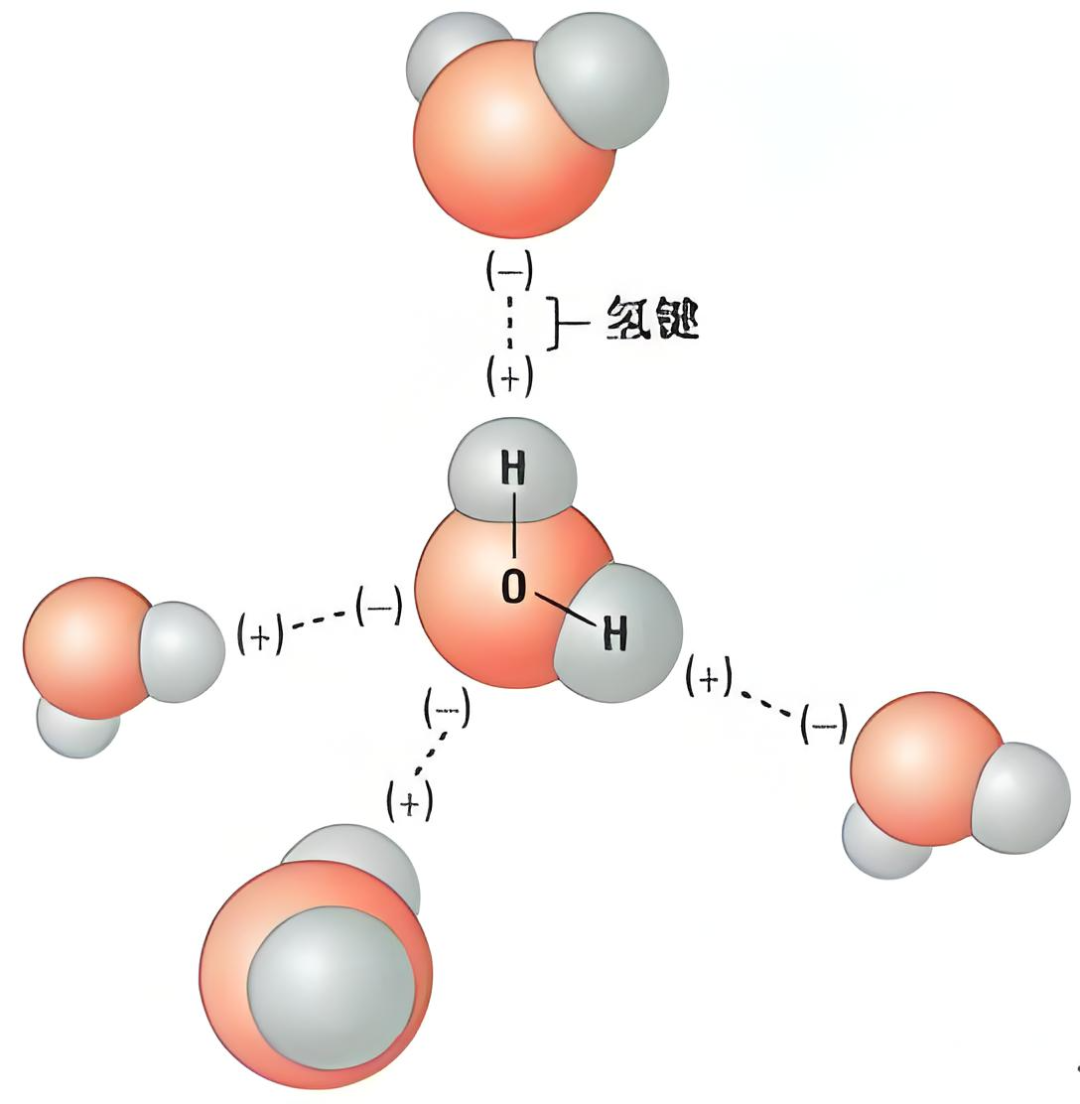
2. 溶解性
氢键影响物质的溶解性。水是极性溶剂,能通过氢键与溶质分子相互作用,因此极性物质易溶于水。例如,乙醇(C₂H₅OH)能与水形成氢键,故易溶于水。
乙醇与水分子形成氢键可参照乙醚与水分子形成的氢键。
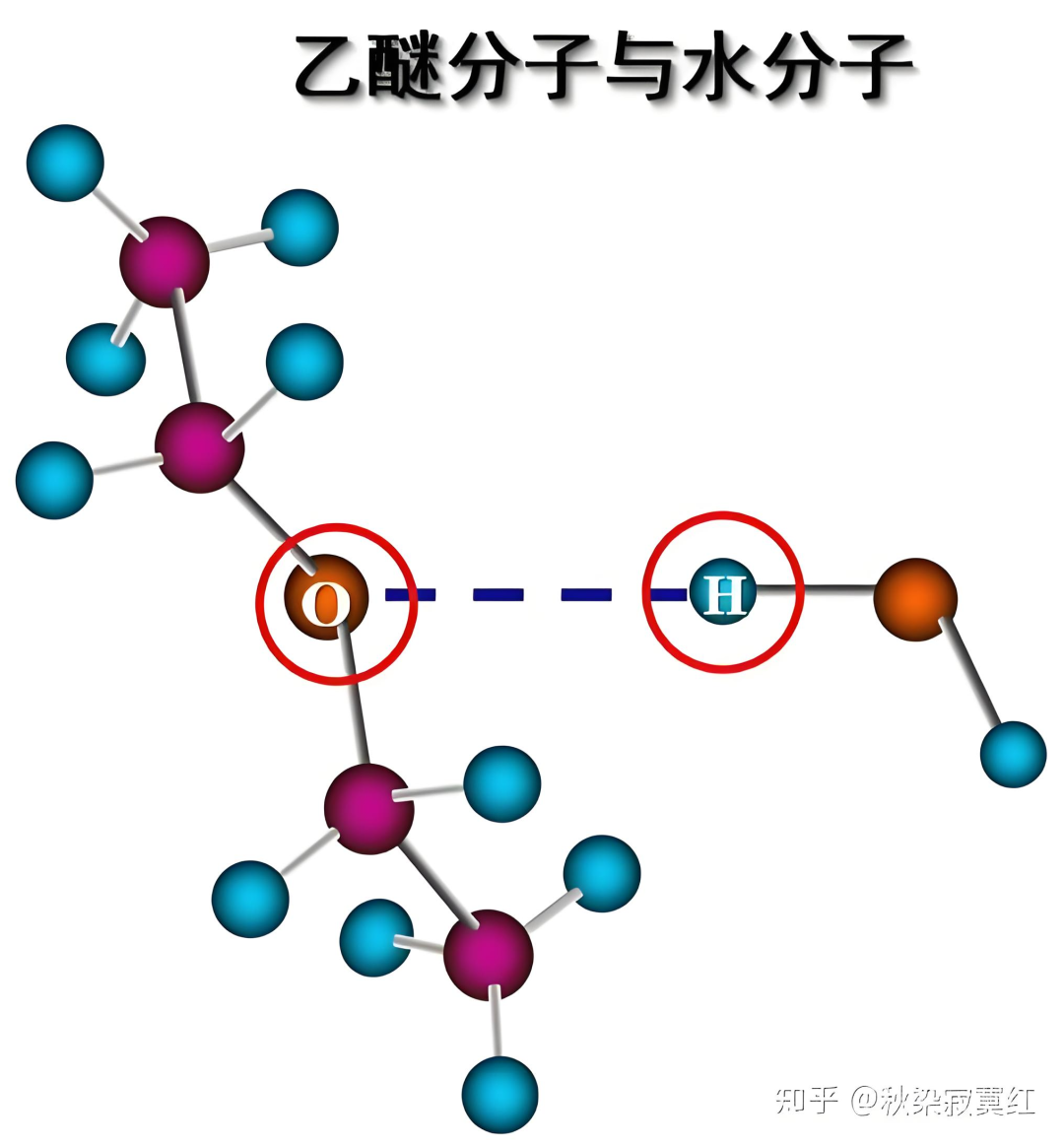
3. 粘度
氢键会增加液体的粘度。例如,甘油的粘度较高,因为其分子间存在多个氢键,阻碍了分子流动。
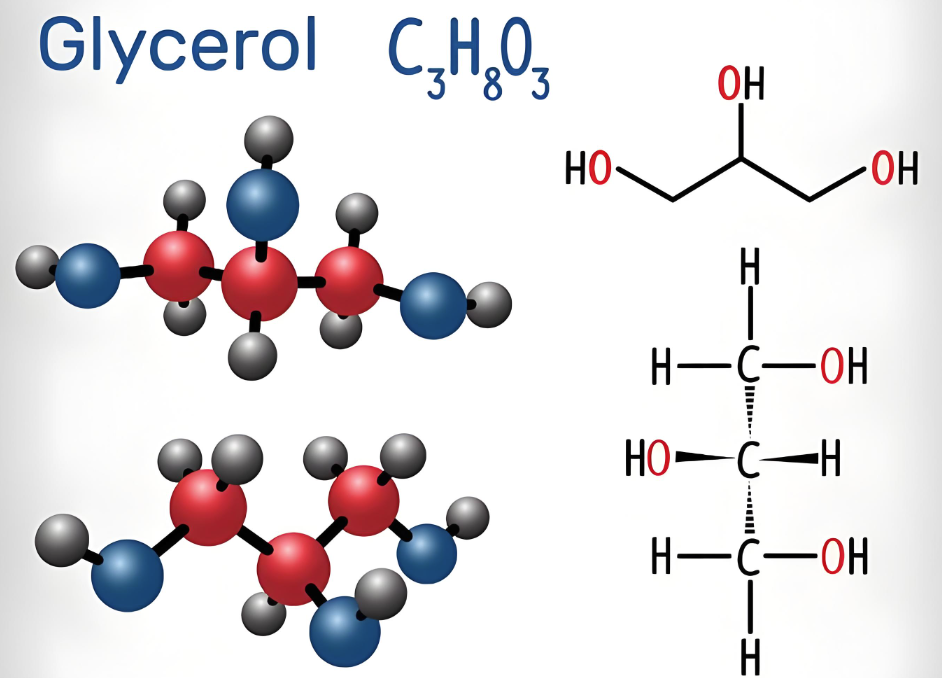
4. 表面张力
氢键能增强液体的表面张力。水的表面张力较高,部分原因是水分子间存在氢键,使得表面分子更紧密地结合在一起。
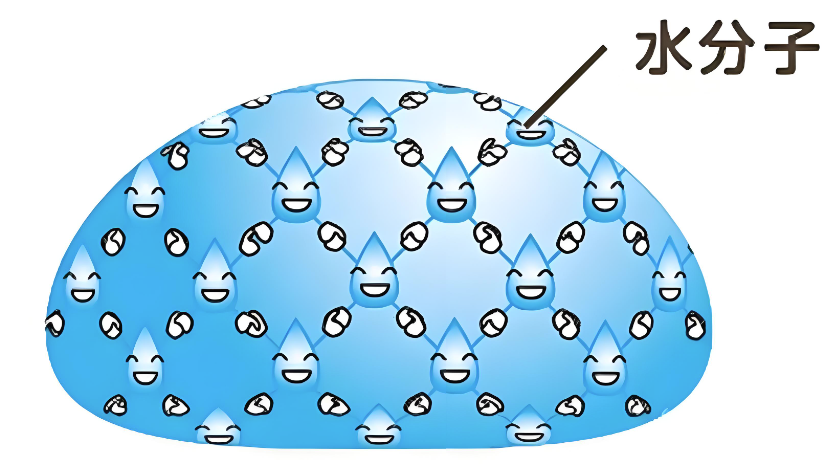
5. 晶体结构
氢键影响晶体的结构。例如,冰的晶体结构中,水分子通过氢键形成四面体排列,导致冰的密度低于液态水。
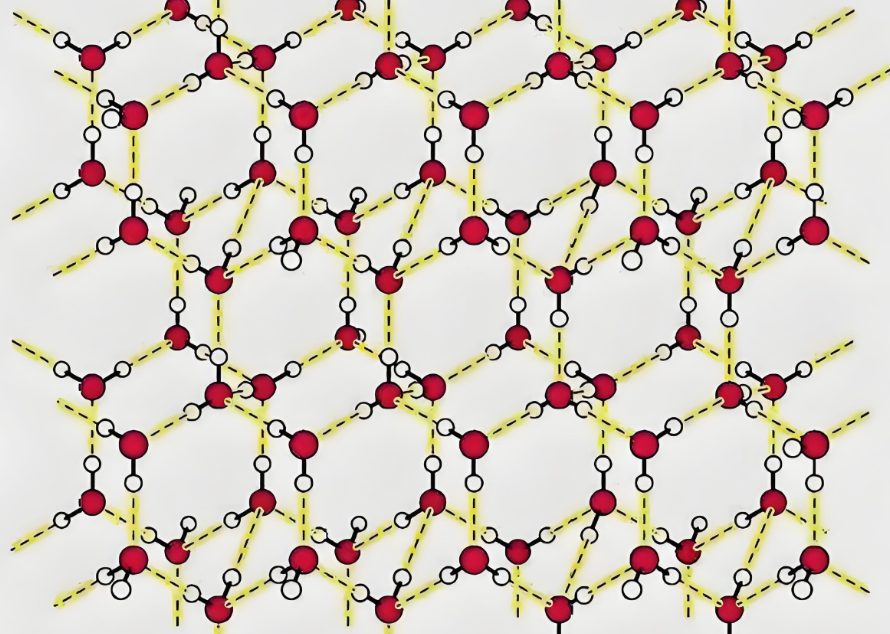
6. 生物分子结构
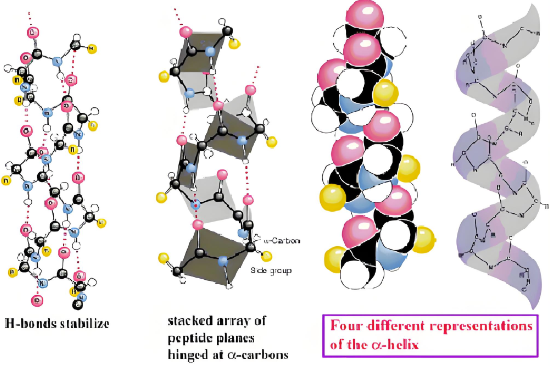
氢键在生物分子中起关键作用。DNA双螺旋结构中,碱基对通过氢键连接;蛋白质的二级结构(如α-螺旋和β-折叠)也依赖氢键维持。
总结
氢键对物质的物理和化学性质有广泛影响,包括沸点、熔点、溶解性、粘度、表面张力、晶体结构以及生物分子的稳定性。理解氢键的作用有助于解释许多自然现象和科学问题。
评论详情