锂离子为什么能在正、负极来回脱嵌?

相信很多人都知道锂离子在充、放电过程中会在正、负极发生脱出和嵌入,但驱动锂离子脱嵌行为的具体原因是什么,可能很多人并不十分了解。
01 充电过程(电能→化学能)

给手机充电
首先,我们使用充电器将外部电源(如家用交流电)转换为适合锂离子电池的直流电压。这个外部电压被施加到电池的正极和负极之间。当外部电压施加到电池上时,电池内部的正极和负极间会形成一个电场。电场是一种物理场,它描述了电荷之间的相互作用力。在锂离子电池中,电场使得正极和负极之间的插层锂离子和其他电荷载体开始移动(就像增大水位差使水流流动一样,增大电压也可加快锂离子迁移)。
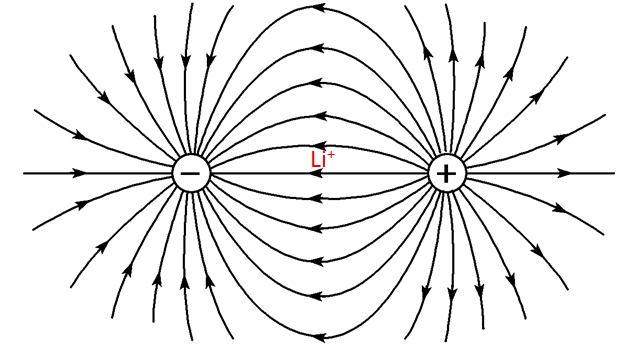
锂离子在电场中迁移
在充电过程中,电场的作用使得插层的锂离子从正极材料中脱出,此时正极多出的电子从正极通过外部电路(即充电器)流向负极,与锂离子结合成锂原子,嵌入石墨层中。正、负电荷在这一过程中实现了平衡。
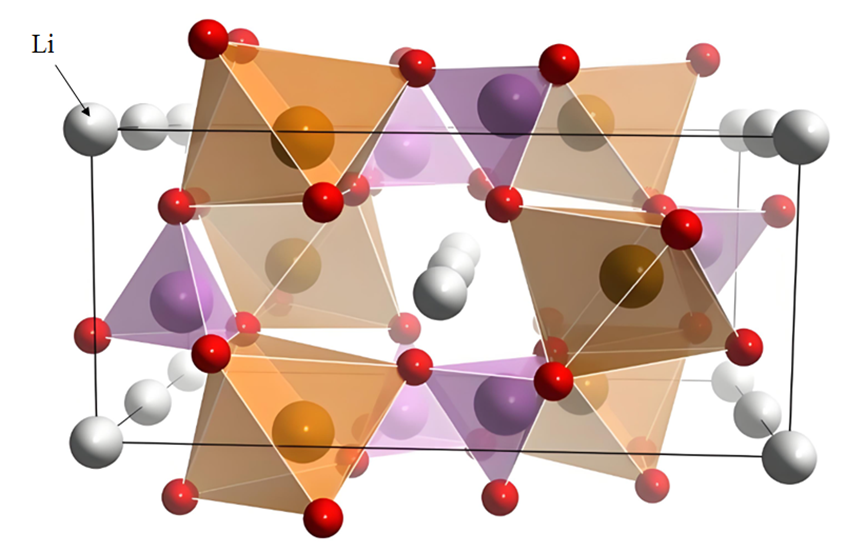
磷酸铁锂中的插层锂离子
(1)锂离子正极固相颗粒中扩散
Li+是从正极颗粒表面脱嵌的,因此正极活性颗粒内部会出现一个Li+的浓度梯度,在这个浓度梯度的驱动下,Li+在正极活性颗粒中发生扩散,这个过程称为固相扩散过程。
正极固相扩散
(2)锂离子在电解液中扩散
由正极颗粒表面电化学反应生成的Li+进入电解液中,溶液相中界面区域的局部浓度提高,使溶液相内部产生浓度差异,导致Li+产生从内向外的扩散与迁移(锂离子就像滴在水中的墨水一样,由浓度高向浓度低扩散)。而在负极区域,由于负极颗粒表面与电解液中的Li+发生电化学反应,消耗了溶液相中的Li+,使溶液相局部Li+浓度降低,产生浓度差异,导致Li+在溶液相中产生由外向内的扩散与迁移。

溶剂化的锂离子发生液相扩散
(3)锂离子负极固相颗粒中扩散
Li+在石墨负极表面发生电化学反应得到一个电子,转变为锂原子,并嵌入到石墨形成锂-碳层间化合物。由于Li+在石墨负极颗粒中扩散速度较慢,因此在嵌锂反应中会在局部首先产生LiC6产物,而其他部分仍然处于贫锂状态,从而在石墨负极内部形成Li的浓度梯度,导致Li从石墨颗粒表面向颗粒中心扩散。
由于锂离子和电子的脱出,正极变得更有电负性,更缺电子,需要更高的电压才能将电子取出。所以在充电时,电池电压变得越来越高。
负极固相扩散
02 放电过程(化学能→电能)
高反应性的锂原子被安全地储存在石墨中。尽管锂原子拥有易于剥离的电子,但这些电子缺乏一个可以转移的接收端。电解液在这个状态下不能导电,而石墨则保持稳定性,拒绝接受额外电子。要实现锂离子的迁移,必须满足两个关键条件:
(1)为电子提供一条通往正极的逃逸通道;
(2)电解液必须准备好接受锂离子。
当正极与负极相连通时,两者之间所有的电子都会感知到一种能量的不均衡状态(电子会从高能级向低能级转移),此时负极最外层的电子向低能级(缺电子)的正极逃离。在负极中,失去电子的锂原子变成锂离子,从负极脱出进入电解液,并向正极扩散和迁移。在正极中,锂离子与来自负极的电子发生反应生成锂原子,重新回嵌入正极。
在反应初期,正极与负极之间的电荷分布极不均衡,电压高达约3.65V(以LFP为例)。随着锂离子逐渐从负极中释放,并被正极所吸收,这种电荷的不均衡状态逐渐得到缓解,电压也随之降低。当电压下降至2.5V时,整个放电循环结束。
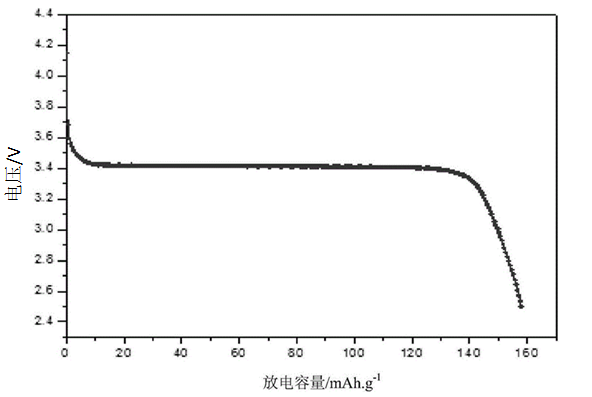
磷酸铁锂(LFP)放电电压曲线
03 启示
由如上所述的锂离子电池充、放电原理可知:凡是能在充电电场作用下实现离子和电子迁移,且不改变正极结构;并在放电时,电子和离子可以自发返回正极,且不改变负极结构的电池系统,均可以称为摇椅电池。
评论详情